Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12113 Beiträge für Sie gefunden
-
GDP-Inspektionen
Rubrik: GxP
(Treffer aus pharmind, Nr. 02, Seite 108 (2026))
GDP-Inspektionen / Häufige Mängel bei der Qualifizierung von Logistikdienstleistern und wie man sie vermeidet – Fortsetzung*Vorheriger Teil s. Pharm. Ind. 87, Nr. 11, 1004–1008 (2025). · Joos L
GDP Inspektion Qualifizierung Mängel Logistikdienstleister Die Aufgaben eines Großhändlers nach § 52a AMG sind in der Arzneimittelhandelsverordnung sowie in der EU-GDP-Leitlinie geregelt. Die zuständige Behörde überprüft die Einhaltung dieser Anforderungen im Rahmen von Inspektionen gemäß § 64 AMG. Im Zuge dieser GDP-Inspektionen stellt die Qualifizierung von Logistikdienstleistern einen wesentlichen Prüfpunkt dar. Dieser Aspekt gewinnt insb. dann an Bedeutung, wenn umfangreiche oder komplexe Tätigkeiten vertraglich an einen (Logistik-)Dienstleister übertragen werden. Neben der Lagerung und dem Transport können Logistikdienstleister weitere Aufgaben übernehmen, etwa die Qualifizierung von Kunden oder die Bearbeitung von Retouren. Die dem Logistikdienstleister übertragenen Tätigkeiten sind im Vertrag mit dem Auftraggeber eindeutig ...
-

Pharma Packaging
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 108 (2026))
Pharma Packaging / Produkte
ACG Packaging Materials presents the cold-form blister technology SuperPod™. This pharma packaging enables blister cavities to become smaller – by up to 39 % according to company information. The cold-form innovation results in a reduced packaging footprint, lower material and resource usage per dosage across the lifecycle, and consequently, reduced costs and carbon emissions. The core innovation behind cold-form blister lies in a multi-layer laminate engineered for cold-drawing capability, enabling deep-draw cavity formation while retaining the full protective properties of cold-form aluminium. A well-designed format also increases the number of blisters per shot – by up to 3 times in some cases ... -

Containerklappen
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 108 (2026))
Containerklappen / Produkte
Warex Valve hat die Containerklappe DKZ 105 SKV für Anwendungen in der Pharmaindustrie entwickelt. Die Armatur dient als Auslaufverschluss für Intermediate Bulk Container(IBC)-Schüttgutcontainer und erfüllt hohe Anforderungen an Hygiene, Dichtheit und Wartungsfreundlichkeit. Weiterhin wird die Containerklappe vollständig aus Edelstahl 1.4404 gefertigt und in totraumarmer Ausführung realisiert. Dadurch werden Produktablagerungen minimiert und Reinigungsprozesse vereinfacht – ein Vorteil für sensible Einsatzbereiche. Ein besonderes Konstruktionsmerkmal ist die speziell ausgeführte Dichtung ohne Störkanten, die einen kontrollierten Materialfluss ermöglicht und gleichzeitig eine hohe Dichtheit sicherstellt. www.warex-valve.com -
Kabeleinführungen
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 108 (2026))
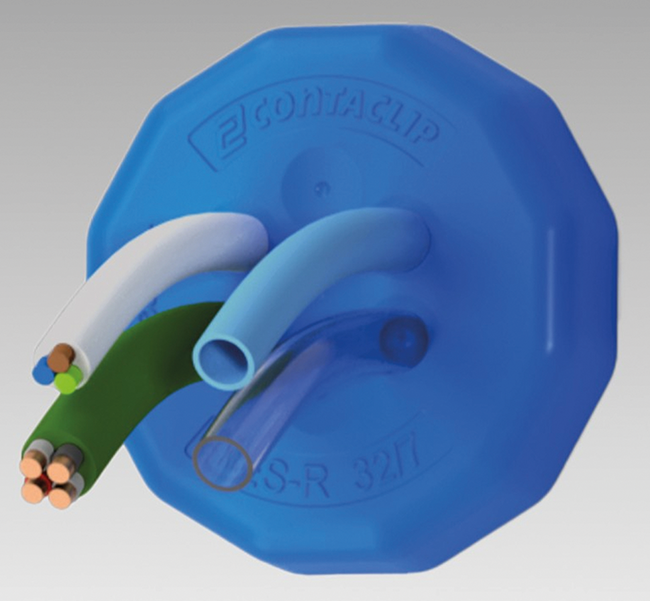
Kabeleinführungen / Produkte
Conta-Clip Verbindungstechnik erweitert kontinuierlich sein Kabeldurchführungsprogramm KES mit einem Augenmerk auf die aus zertifiziertem, hygienischem Material gefertigten Ausführungen für die Pharmaindustrie. In diesem Kontext entstand auch die in charakteristischem Blau gehaltene runde FDA-Variante von KES-R-FDA M. Diese Kabeleinführung ermöglicht eine schnelle und platzsparende Einführung von bis zu 68 Leitungen in Schaltschränke oder Maschinengehäuse. Zudem erfüllt das Produkt durch glatte Oberflächen und abgerundete Ecken die geforderten Hygieneeigenschaften in der Pharmaindustrie. Das Unternehmen bietet die FDA-Kabeleinführungen KES-R-FDA M aktuell in 15 runden Varianten für unterschiedliche Leitungsanzahlen und -durchmesser an. conta-clip.com -

Produktinspektionen
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 109 (2026))
Produktinspektionen / Produkte
Mettler Toledo hat die neuen Röntgeninspektionssysteme der X3-Serie für Schüttgüter vorgestellt. Diese Systeme sind auf eine Fremdkörpererkennung (Größe 0,3 mm bis 0,4 mm) und eine vereinfachte Bedienung ausgelegt. Die aus den Modellen X13 und X53 bestehende X3-Serie basiert auf der X2-Systemfamilie mit vereinheitlichten Komponenten. Sie zeichnet sich durch ein hygienisches Design aus. Die X3-Serie wurde speziell für unverpackte, lose Schüttgüter auf Transportbändern entwickelt. Typische Anwendungen sind u. a. Tabletten, Pillen und kleine Beutel. Die Ausschleusoptionen umfassen einen Mechanismus mit 30 Blasdüsen zum Entfernen von Fremdkörpern aus kleineren Produkten und einen Pusher mit 6 Klappen zur Ausschleusung von Fremdkörpern aus größeren Produkten. www.mt.com -

Schraubenspindelpumpen
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 109 (2026))
Schraubenspindelpumpen / Produkte
Jung Process Systems bietet Schraubenspindelpumpen der Marke HYGHSPIN an. Die Pumpen zeichnen sich durch hohe Effizienz, Flexibilität und Langlebigkeit aus. Alle Bauteile und die Pumpen selbst werden nach Herstellerangaben ausschließlich am Standort Kummerfeld gefertigt und montiert. Die zentralen Erfolgsfaktoren sind neben dem wirtschaftlichen Erfolg die Qualität, attraktive Lieferzeiten, der gute Service und die innovativen Fertigungsprozesse. Kontinuierliche Investitionen in moderne Fertigungstechnik bei Jung & Co. ermöglichen es den steigenden Kundenanforderungen global gerecht zu werden und Wachstumspotenziale nachhaltig zu nutzen. www.jung-process-systems.de -

Non-contact Flow Meter
Rubrik: Produkte
(Treffer aus Tech4Pharma, Nr. 02, Seite 109 (2026))
Non-contact Flow Meter / Produkte
With the SONOFLOW CO.55 SD V3.0, ultrasonic specialist SONOTEC has developed the world's first non-contact flow meter – according to its own company information. The flow meter has integrated color touch display and stainless steel housing for single-use applications in GMP bioprocessing. Designed with a special focus on low flow bioprocessing applications, the ultrasonic clamp-on flow sensor combines good measurement accuracy over a wide flow range and high clamp-to-clamp repeatability. With a measuring accuracy of 1 %, the non-contact flow meter offers highly accurate and reliable flow measurement. The sensors are easily clamped on the tubing and measure without contact to the media ... -

2 Wechsel bei Hosokawa Alpine
Rubrik: Personen
(Treffer aus Tech4Pharma, Nr. 02, Seite 110 (2026))
2 Wechsel bei Hosokawa Alpine / Personen | Unternehmen
Im Jan. 2026 gab es bei Hosokawa Alpine 2 Wechsel in der Unternehmensführung. Die bisherigen Vorstände Dr. Antonio Fernández (CEO) und Jürgen Wilde (CFO/COO) haben ihre Ämter niedergelegt. Ihre Nachfolge übernahmen Michael Kuhnen als neuer Chief Executive Officer (CEO) und Kathrin Dörle als neue Chief Financial Officer (CFO). Kuhnen wird künftig die strategische Weiterentwicklung von Hosokawa Alpine vorantreiben und ist u. a. für die vertrieblichen und operativen Bereiche sowie die internationalen Niederlassungen verantwortlich. Dörle übernimmt die Bereiche Finanzen und Corporate Center. -

RAUMEDIC erweitert Vorstand
Rubrik: Personen
(Treffer aus Tech4Pharma, Nr. 02, Seite 110 (2026))
RAUMEDIC erweitert Vorstand / Personen | Unternehmen
RAUMEDIC hat im Jan. 2026 Bianca Holler als Chief Human Resources Officer (CHRO) in den Vorstand berufen. Mit der Erweiterung des Führungsgremiums um eine eigenständige Vorstandsposition für Personal unterstreicht das Medizin- und Pharmatechnikunternehmen die strategische Bedeutung seiner Mitarbeitenden für den Unternehmenserfolg. Holler ist seit Mai 2023 Teil von RAUMEDIC und hat in ihrer bisherigen Funktion als Global Vice President Human Resources bereits zur strategischen Weiterentwicklung der Personalarbeit beigetragen. Unter ihrer Verantwortung hat das Unternehmen die Personalarbeit strategisch neu aufgestellt: von der Modernisierung der Leistungsbeurteilung über die Weiterentwicklung der Führungskultur bis hin zur systematischen Messung und Verbesserung der Mitarbeiterzufriedenheit. -

Neuer Geschäftsführer bei ViscoTec
Rubrik: Personen
(Treffer aus Tech4Pharma, Nr. 02, Seite 110 (2026))
Neuer Geschäftsführer bei ViscoTec / Personen | Unternehmen
Im Jan. 2026 hat Franz Kamhuber von Martin Stadler die Geschäftsführung bei ViscoTec übernommen. Nach 23 Jahren im Unternehmen verließ der bisherige technische Geschäftsführer Stadler ViscoTec. Die Gesamtverantwortung übernahm danach der bisherige kaufmännische Geschäftsführer Kamhuber, der damit für Kontinuität und Stabilität in der Führung steht. Gleichzeitig stärkte ViscoTec seine Managementstruktur: Mit dem Ausscheiden von Stadler wurden die beiden Bereichsleiter Josef Donislreiter und Florian Wagner mit Einzelprokura ausgestattet. Gemeinsam mit Kamhuber bilden diese beiden künftig das Management Board. Das Unternehmen ist ein Spezialist für Dosiertechnik und beschäftigt mehr als 350 Mitarbeitende.
Sie sehen Artikel 12001 bis 12010 von insgesamt 12113
- Erste Seite
- 1199
- 1200
- 1201
- 1202
- 1203
- Letzte Seite





