Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12086 Beiträge für Sie gefunden
-

Europa im Rückstand?
Rubrik: Statements der Verbände
(Treffer aus pharmind, Nr. 01, Seite 10 (2024))
Europa im Rückstand? / Warum die pharmazeutische Industrie vom Spielfeld auf die Ersatzbank gezwungen wird · Herzog A · Generalsekretär der PHARMIG – Verband der pharmazeutischen Industrie Österreichs
Buhrufe und Jubel wird es 2024 gleichermaßen und in allen Teilen Europas geben. Dann nämlich, wenn Fußballfans die Europameisterschaft feiern. Wer dabei nicht im öffentlichen Fokus stehen wird, ist der Rasen bzw. das Spielfeld. Wiewohl dieses eine wichtige Voraussetzung für ein gutes Spiel ist. Schließlich nimmt es je nach Beschaffenheit und Wetterlage Einfluss auf den Spielverlauf. Das Spiel selbst erscheint wichtiger als der Boden, auf dem es stattfindet. Aber der Erfolg hängt vom Zusammenwirken aller Faktoren ab. Und das gilt nicht nur für ein Fußballspiel, sondern auch für den Standort Europa. Wie, das möchte ich im Detail beleuchten. Bleiben wir ...
-
Bewährungsprobe für Reinraumbekleidung
Rubrik: Ausstattung
(Treffer aus cleanroom & processes, Nr. 01, Seite 10 (2024))
Held-Föhn E | Schmeer-Lioe G | Linti C | Stegmaier T | Gresser G | Kopp A | Moschner C | Gaza S
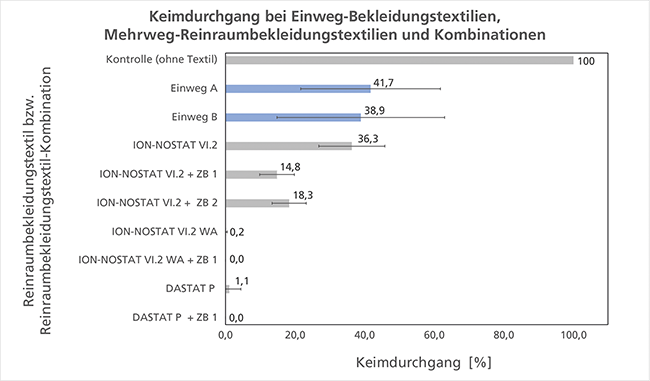
Bewährungsprobe für Reinraumbekleidung / Die ReBa2-Prüfmethode zur Bestimmung des Keimdurchgangs – Teil 2*Teil 1 dieses Beitrags s. cleanroom & processes 2023;2(4): 174–178. · Held-Föhn E, Schmeer-Lioe G, Linti C, Stegmaier T, Gresser G, Kopp A, Moschner C, Gaza S · Deutsche Institute für Textil- und Faserforschung Denkendorf, Denkendorf und Dastex Reinraumzubehör GmbH & Co. KG, Muggensturm und und
Die quadratischen Messproben werden zugeschnitten, die Außen- bzw. Innenseite markiert und sterilisiert. Das Sterilisationsverfahren wird vorzugsweise entsprechend der geplanten Anwendung ausgewählt, z. B. Dampfsterilisation. Bei Materialien, die bereits in sterilem Zustand geliefert werden, ist eine aseptische Messprobenentnahme möglich. Die Komponenten Baumwollgewebe, Keimträger- sowie Abdeckfolie werden dampfsterilisiert. Das Prüfgerät wird vor dem Einsatz und nach Versuchsende (vorzugsweise mit alkoholischem Desinfektionsmittel) desinfiziert. Jede Keimträgerfolie wird in einer markierten Fläche mit Staphylococcus-epidermidis -Suspension mit einer Endkonzentration von (0,5–2,0) x 10 5 KBE beaufschlagt. Die Bakteriensuspension wird homogen bis zur Trocknung auf dem Keimträger verteilt. An den 6 Prüfstellen werden jeweils (wie in Teil I dieses Beitrags beschrieben) die ...
-

Die Patientinnen und Patienten gehören in den Mittelpunkt
Rubrik: Statements der Verbände
(Treffer aus pharmind, Nr. 01, Seite 8 (2024))
Die Patientinnen und Patienten gehören in den Mittelpunkt / pharmind • Statements der Verbände · Buholzer R · Geschäftsführer und Delegierter des Vorstandes Interpharma iph
Die Schweiz hat Ende Okt. 2023 ein neues Parlament gewählt. Was die parteipolitische Zusammensetzung angeht, so erfuhr diese – nach einem fulminanten Gewinn der grünen Partei vor 4 Jahren – eine Korrektur zugunsten der bürgerlich-konservativen Parteien. Turnusgemäß folgten nach den Parlamentswahlen Mitte Dez. die Bundesratswahlen, also die Wahl der 7 Regierungsmitglieder. Von der Pharmabranche mit Spannung erwartet wurde die Bekanntgabe der neuen Departementsleitung, die auf Bundesrätin Elisabeth Baume-Schneider gefallen ist. Auf sie warten im Jahr 2024 große Herausforderungen, die es zu lösen gilt. Ebenfalls stimmen die Schweizer Stimmbürgerinnen und Stimmbürger im Juni über 2 Initiativen ab, die potenziell stark mobilisieren und die Aufmerksamkeit ...
-

Schlüsselindustrie Pharma als Chance für den Wirtschaftsstandort
Rubrik: Statements der Verbände
(Treffer aus pharmind, Nr. 01, Seite 6 (2024))
Schlüsselindustrie Pharma als Chance für den Wirtschaftsstandort / pharmind • Statements der Verbände · Steutel H · Präsident des vfa – Die forschenden Pharma-Unternehmen
Deutschland steckt mitten in einer grundlegenden Transformation. Die Umstellung auf klimaneutrale Energieerzeugung hat durch die gestiegenen Energiepreise in Folge des russischen Angriffskriegs auf die Ukraine weiter an Dynamik gewonnen. Damit verschieben sich die Wettbewerbsbedingungen einzelner Branchen, was den Aufstieg neuer Wirtschaftszweige begünstigt. Derzeit kommen mehrere grundlegende Änderungen zusammen: Die Digitalisierung verändert Produktions- und Innovationsprozesse fundamental. Die Energiewende erfordert andere Produktionstechnologien. Die Demografie verknappt den Faktor Arbeit in den kommenden Jahren erheblich. In einem höchst fragilen geopolitischen Umfeld steht Deutschland vor einem massiven Strukturwandel. Wirtschaftssysteme unterliegen fortwährenden Änderungen. Der Wandel von tradierten Wirtschaftsmodellen mit historisch gewachsenen Wertschöpfungsstrukturen erfordert einen ambitionierten Umbau ...
-

Arzneimittelversorgung und Pharmastandort stärken bevor der Zug abgefahren ist
Rubrik: Statements der Verbände
(Treffer aus pharmind, Nr. 01, Seite 4 (2024))
Arzneimittelversorgung und Pharmastandort stärken bevor der Zug abgefahren ist / pharmind • Statements der Verbände · Joachimsen K · Hauptgeschäftsführer BPI – Bundesverband der Pharmazeutischen Industrie e. V. (BPI)
2023 war das Jahr der Lieferengpässe und zugleich der verpassten Chancen. Als plötzlich Kinderarzneimittel betroffen waren, konnte es gesetzestechnisch gar nicht schnell genug gehen. Wir konnten die Politik überzeugen, dass es einen klaren Zusammenhang zwischen zu niedrigen Preisen, Marktverengung und Lieferengpässen gibt. „Wir haben es mit der Ökonomisierung übertrieben. Die Krankenkassen haben die Preisspirale überdreht und dafür gesorgt, dass immer nur die allerbilligsten Hersteller berücksichtigt wurden.“, erkannte Bundesgesundheitsminister Karl Lauterbach richtigerweise. Und er nährte damit die Hoffnung auf einen großen Wurf, auf eine echte Reform in der Grundversorgung, welche bereits in der letzten Legislaturperiode – trotz gleicher Entwicklung – ausblieb. ...
-
No-Touch Transfer (NTT)
Rubrik: Reinraum
(Treffer aus Tech4Pharma, Nr. 01, Seite 4 (2024))
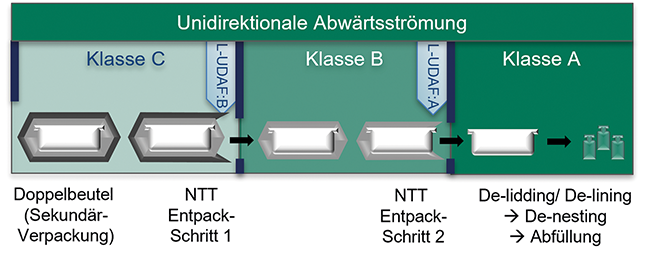
No-Touch Transfer (NTT) / Eine schlanke Lösung zur Einbringung vorsterilisierter Primärpackmittel in den Klasse-A-Bereich · Scharf B, Negro E · Franz Ziel GmbH, Billerbeck und Zicura Pharma Solutions GmbH, Nordhorn
Aseptische Prozesse Kontaminationskontrolle No-Touch Transfer (NTT) Qualifizierung Vorsterilisiertes Verpackungsmaterial In der pharmazeutischen Industrie hat das Interesse an der Verwendung vorsterilisierter Primärverpackungen bei der aseptischen Abfüllung von sterilen Arzneimitteln stark zugenommen [ 1 , 2 ]. Auch die Lohnabfüller müssen flexibel reagieren und den Anforderungen der Abfüllung kleiner bis mittlerer Chargen gerecht werden, sodass sich vorsterilisierte Vials und Spritzen als neuer Industriestandard etabliert haben [ 3 ]. In diesem Zusammenhang wurde das Konzept des No-Touch Transfer (NTT) als innovatives Verfahren entwickelt, das die Einführung vorsterilisierter Primärverpackungsmaterialien in den Klasse-A-Bereich ermöglicht. Unter Einhaltung der Good-Manufacturing-Practice(GMP)-Regularien einschließlich des Qualitätsrisikomanagements (QRM) [ 4 ] ...
-
Schutz von kritischen Komponenten vor Oberflächenkontaminationen
Rubrik: Ausstattung
(Treffer aus cleanroom & processes, Nr. 01, Seite 4 (2024))
Kopp A | Moschner C | Müller A
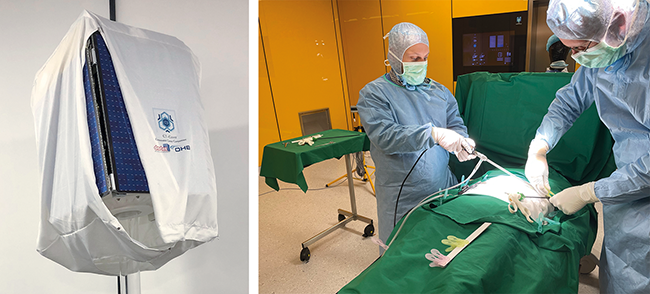
Schutz von kritischen Komponenten vor Oberflächenkontaminationen / Teil 1 · Kopp A, Moschner C, Müller A · Dastex Reinraumzubehör GmbH & Co. KG, Muggensturm und OHB System AG, Bremen
Abdeckungen Kontamination Risikobewertung Reinraumtextilien Nachhaltigkeit In allen Bereichen kommt es, je nach Umgebungsbedingungen, zur zeitlichen Ablagerung von luftgetragenen Kontaminationen. Dies gilt auch für kontrollierte Umgebungsbedingungen – wie in Reinräumen. Die Luft in Reinräumen wird zwar gefiltert und überwacht; trotzdem lagern sich auch hier über die Zeit Kontaminationen auf kritischen Komponenten, Produkten und Oberflächen ab. Daher ist es gängige Praxis, diese je nach Prozessanforderungen mit Abdeckungen davor zu schützen. Um die geforderte Oberflächenreinheit unter einer solchen Abdeckhaube sicherzustellen, sind Material, Geometrie und Dichtigkeit ausschlaggebende Faktoren. Unter der Voraussetzung, die richtige Abdeckung ausgewählt zu haben, schützt diese die darunter befindlichen Objekte bzw. ...
-

Besserung in Sicht?
Rubrik: Statements der Verbände
(Treffer aus pharmind, Nr. 01, Seite 2 (2024))
Besserung in Sicht? / pharmind • Statements der Verbände · Cranz H · Hauptgeschäftsführer des Bundesverbandes der Arzneimittel-Hersteller e. V. (BAH)
Gesundheit fällt nicht vom Himmel, wir müssen etwas dafür tun – jeder Einzelne für sich und wir alle für uns alle. Somit erfordert Gesundheit Engagement und auch Investitionen. Sicherheit, die ökologische und digitale Transformation unserer Wirtschaft und Gesellschaft, Bildung aber eben auch Gesundheit, das alles sind zentrale Bereiche, die finanziellen Einsatz benötigen, der auch in Zeiten knapper Ressourcen gerechtfertigt ist. Wichtig ist dabei eine durchdachte Politik mit sozialökonomischem Sachverstand und eine Anerkennung der Rolle des Arzneimittels, das ein wichtiger Teil der Gesundheitsversorgung ist und wesentlich zu einem resilienten Gesundheitssystem beiträgt. Wir sollten für eine sichere und finanzierbare Gesundheitsversorgung nicht am, ...
-

Keiner weiß alles!
Rubrik: Editorial
(Treffer aus cleanroom & processes, Nr. 01, Seite 1 (2024))
Keiner weiß alles! / Editorial
Sehr geehrte Leserinnen und Leser, vor einiger Zeit, im Gespräch mit einem Experten und späteren Autor eines Fachbeitrags, waren wir verblüfft. Es ging um Sensoren und deren Einsatz, und wir wunderten uns, weshalb diese Sensoren nicht auch im Reinraum angewendet wurden. Noch verblüffter war der Experte, der auf unsere Nachfrage hin zugeben musste, an diese Querschnittsbranche gar nicht gedacht zu haben. Für ihn eröffnete sich ein neues Einsatzgebiet – und wir kamen später zu einer spannenden Case Study. Win-Win! Was lernen wir? Gespräche öffnen uns die Augen, nicht jeder Aspekt kann immer vorausgesetzt werden. Und weil das so neu gar ... -

Wenn man erst einmal einen Namen hat, ist es ganz egal, wie man heißt.
Rubrik: Editorial
(Treffer aus Tech4Pharma, Nr. 01, Seite 1 (2024))
Wenn man erst einmal einen Namen hat, ist es ganz egal, wie man heißt. / Editorial
Sehr geehrte Leserinnen und Leser, Sie halten die erste Ausgabe der Tech4Pharma (vormals TechnoPharm) in Händen. Sie bemerken keinen inhaltlichen Unterschied zu früheren Ausgaben? Dann ist unser Plan aufgegangen. Denn viel wichtiger als der Name war und ist uns der beiratsgeprüfte Inhalt, für den wir seit der Gründung des Titels vor 14 Jahren viel Zustimmung erfahren haben. APV-Mitgliedern wird auffallen, dass nun keine APV-News mehr im Heft zu finden sind – so wollte es der Vereinsvorstand. Für die Fach-Redaktion entsteht nun mehr Platz für mehr Berichte aus der Industrie. Diese Ausgabe widmet sich dem Fokus Pharmaproduktion/-automation. Hierbei sticht besonders der ...
Sie sehen Artikel 1081 bis 1090 von insgesamt 12086
- Erste Seite
- 107
- 108
- 109
- 110
- 111
- Letzte Seite