Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12113 Beiträge für Sie gefunden
-

Reinräume
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 114 (2024))
Reinräume / Produkte
Die vorgefertigten Standard-Reinräume von Viessmann Technologies *) bieten eine Alternative zu einem konventionellen Neubau, der kostspieligen Renovierung oder dem Umbau eines bestehenden Gebäudes. Die Standard-Reinräume sind dank Plug-and-Play-Lösungen flexibel und durch die Modularität können sie jederzeit an einem anderen Ort wiederaufgebaut werden. Die Reinräume können für die Reinheitsklassen D–A des EU-GMP-Leitfadens geliefert werden. Ihre Gestaltung erfüllt die gültigen Standards und Richtlinien der Reinraumtechnik. Alle vorgefertigten Reinräume beinhalten: getestete mikrobizide Oberflächen dauerhafte Resistenz gegen Reinigungs- und Desinfektionsmittel und gegen H 2 O 2 -Begasung autarke Infrastruktur mit Einzelbelüftung, alternativ Zentralversorgung Klimatisierung, Zuluft über deckenintegrierte LF-Module Druckhaltung von –60 bis +120 Pa ... -

Analysegeräte
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 114 (2024))
Analysegeräte / Produkte
Festo *) hat zusammen mit der C. Gerhardt GmbH & Co. KG in Königswinter das automatisierte Stickstoff-Analysegerät N-Realizer entwickelt. Das Laborgerät sorgt für hohen Durchsatz, ist wartungsarm und intuitiv zu bedienen. Das verdankt es u. a. einem Ventilblock von Festo, der mit hoher Dichtigkeit bei der Gasverteilung aufwartet. Der Ventilblock mit den mediengetrennten Magnetventilen VYKA hilft dabei das Kohlendioxid über die Adsorberanlage zu entfernen. Die individuell erstellte Kundenlösung verteilt Proben- und Spülgas in den CO 2 -Fallen. Dabei bietet die eingesetzte Dumas-Methode Vorteile gegenüber der nasschemischen Kjeldahl-Methode: Sie ist schneller, erfordert weniger Vorbereitungen und ist für die Laboranten sicherer, da ... -

Reinigungsanlagen
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 114 (2024))
Reinigungsanlagen / Produkte
Getinge *) präsentiert mit dem GEW 888 neo eine cGMP-Reinigungsanlage, welche die Effizienz im Reinraum steigern soll. Durch die Kombination einer kleineren Stellfläche mit hoher Reinigungskapazität können biopharmazeutische Unternehmen ihre Installation optimieren. Der GEW 888 neo verfügt über einen reduzierten Wasser- und Energieverbrauch. Die robuste Konstruktion und die Verwendung hochwertiger Komponenten versprechen eine lange Lebensdauer und minimieren Ausfallzeiten. Die intuitive Touchscreen-Bedienoberfläche und das zusätzliche Laderegal-Identifizierungs- und AutoStart-System verbessern die Handhabung durch den Bediener. Die vertikale, platzsparende Schiebetür ermöglicht ein ergonomisches Be- und Entladen des Beladegestells. Der GEW 888 neo verfügt über ein IO-Link-System – ein Kommunikationsprotokoll für Sensoren und Stellantriebe, die über Feldbusverbindungen angeschlossen sind. ... -

Destillations- und Dampferzeugungsanlagen
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 115 (2024))
Destillations- und Dampferzeugungsanlagen / Produkte
Veolia Water Technologies *) hat die neueste Generation von Polaris™ zur Erzeugung von Water For Injection (WFI) und Reindampf auf den Markt gebracht: die auf Gestellen montierten Systeme Polaris™ 2.0 Multiple Effect Distiller (MED) und Polaris™ 2.0 Pure Steam Generator (PSG). Polaris™ 2.0 umfasst eine Auswahl von Standardanlagen mit unterschiedlichen Kapazitäten und mehreren Optionen. Diese erfüllen den ASME-Bioprocessing-Equipment(BPE)-Standard und durch das Siemens HMI Comfort Panel mitsamt neuer, validierter und zertifizierter Software FDA 21 CFR Part 11 und GAMP V. Außerdem sind die Systeme mit der cloudbasierten Fernüberwachungs- und Optimierungslösung Hubgrade von Veolia kompatibel. Die Polaris™-2.0-MED haben Kapazitäten von 300 l/h bis 3 800 l/h und ... -

Isolatormodule
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 115 (2024))
Isolatormodule / Produkte
Das von Bausch + Ströbel *) neu entwickelte Modul SFM 5205 füllt und verschließt RTU-Objekte (Spritzen und Karpulen), ohne dass dafür das Modul gewechselt werden muss. Das De- und Renesten übernimmt das angeschlossene VarioSys-Modul DDM. Flexibilität bietet das SFM auch im Bereich des Dosierens: wählbar sind unterschiedlichste Dosiersysteme wie Peristaltikpumpen, Drehkolbenpumpen oder ein Zeit-Druck-Dosiersystem. Auch das bewährte Multi-Dosiersystem ist möglich. Bis zu 4 500 Objekte pro h werden ausgebracht. Das neu entwickelte Modul bietet dabei eine Inprozesskontrolle (IPC) für jedes einzelne Objekt, ohne dass sich dies negativ auf die Leistung auswirkt. Es gibt kein über- oder unterdosiertes Objekt (Advanced Fill) und auch die Stopfenposition kann ... -

Reinstdampfsysteme
Rubrik: Produkte
(Treffer aus cleanroom & processes, Nr. 02, Seite 115 (2024))
Reinstdampfsysteme / Produkte
Die EnviroFALK *) Reinstdampferzeuger stellen qualifizierten Reinstdampf für die Sterilisation von Komponenten, Rohrleitungen und medizinischen Geräten gemäß den strengen Anforderungen aller gängigen Arzneibücher her. Zur Einhaltung der EN 285 können die Systeme mit einer thermischen Entgasung zur Entfernung sog. „nicht kondensierbarer Gase“ des Speisewassers ausgestattet werden. Durch die außenliegenden Wärmetauscher sind Serviceeinsätze schnell und effizient durchzuführen. Zudem sorgt die geringe Aufstiegsgeschwindigkeit des Dampfes innerhalb der Druckkolonne für eine optimale Tröpfchenabscheidung (Endotoxin kontrollierter Reinstdampf). EnviroFALK setzt bei der Reinstdampferzeugung auf hohe Qualitätsstandards in der Auswahl von Materialien und Komponenten, sowie einen effizienten Prozess. -
PUPSIT – Umsetzung der Anforderungen aus dem neuen EU-GMP-Annex 1
Rubrik: GMP / GLP / GCP
(Treffer aus pharmind, Nr. 02, Seite 118 (2024))
PUPSIT – Umsetzung der Anforderungen aus dem neuen EU-GMP-Annex 1 / Schulze und Biel • PUPSIT · Schulze R1, Biel S2 · 1Sächsisches Staatsministerium für Soziales und gesellschaftlichen Zusammenhalt, Dresden und Merck Life Science KGaA, Darmstadt
Annex 1 Sterilfiltration Filterintegritätstest PUPSIT Filtervalidierung Zu Beginn zunächst eine Quizfrage: Die meistdiskutierte Anforderung des neuen EU-GMP-Annex 1 ist a) so anspruchsvoll, dass sie erst ab Ende 2024 erfüllt werden muss, b) der rote Faden, der sich durch alle Kapitel dieses Dokuments zieht, oder c) ein alter Hut. Klar, die richtige Antwort hängt davon ab, was man als „die meistdiskutierte Anforderung“ ansieht. Fällt die Wahl auf das Design, die Beladung und die Sterilisation von Gefriertrocknern, wäre a) richtig. Wer „Kontaminationskontrollstrategie“ (Contamination Control Strategy, CCS) und „Qualitätsrisikomanagement“ (QRM) bevorzugt, würde auf b) tippen. Die allermeisten Kolleginnen und Kollegen, die von den Autoren der vorliegenden ...
-
Ein Validierungskonzept für KI-Systeme in der Pharmaproduktion
Rubrik: IT
(Treffer aus Tech4Pharma, Nr. 02, Seite 118 (2024))
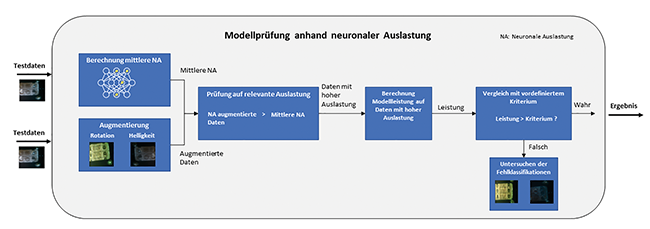
Ein Validierungskonzept für KI-Systeme in der Pharmaproduktion / Teil 2*Teil 1 dieses Beitrags ist erschienen in Tech4Pharma 14, Nr. 1, 50–55 (2024). · Charizanis A, Mettler H · Reichenbach an der Fils, Stuttgart und Exyte Central Europe GmbH
Um den Threshold für die Beurteilung der Verteilungszugehörigkeit zu berechnen, stellt der Prüfer sowohl einen validen Datensatz als auch einen invaliden Datensatz mit einer überschaubaren Anzahl an Testdaten bereit. Für jedes einzelne Bild wird anschließend die Wahrscheinlichkeit zur Verteilungszugehörigkeit berechnet. Diese Sätze an Wahrscheinlichkeiten werden mithilfe des Boot-Strap-Verfahrens künstlich vermehrt, um so eine erhöhte statistische Aussagekraft zu erhalten. Durch das Aufstellen eines Konfidenzintervalls werden 2 Grenzwerte festgelegt. Die untere Grenze des validen Datensatzes beschreibt, welchen Wert valide Daten mit einem bestimmten Wahrscheinlichkeitsgrad mindestens besitzen. Die obere Grenze des invaliden Datensatzes hingegen legt fest, welchen Wert invalide Daten mit einer bestimmten Wahrscheinlichkeit ...
-

35 Jahre ZETA
Rubrik: Partner der Industrie
(Treffer aus Tech4Pharma, Nr. 02, Seite 123 (2024))
35 Jahre ZETA / Partner der Industrie
ZETA wurde 1989 in Graz (Österreich) von Gerhard Zehetner und Manfred Tabor als Planungsbüro gegründet. Der Name des Unternehmens setzt sich aus den Anfangsbuchstaben der beiden Gründer zusammen. ZETA hat sich die Beschleunigung der Prozesse zur Markteinführung lebenswichtiger Medikamente zur Mission erklärt und ist in den letzten 12 Jahren zu einem Weltmarktführer im Bereich Prozesstechnologie für biopharmazeutische Produktionsanlagen aufgestiegen. Diese rasante Entwicklung nahm 2011 ihren Ausgang: Als Karl-Franz Maier, Alfred Marchler, Doris Maier und Andreas Marchler das Unternehmen gekauft hatten, war ZETA eine Firma mit 120 Mitarbeitenden und einem eingeschränkten Portfolio. Das hat sich gründlich geändert: Die ZETA Gruppe ist heute ein ... -
cGMP-konforme Reinigungsprozesse und deren Validierung
Rubrik: GMP / GLP / GCP
(Treffer aus pharmind, Nr. 02, Seite 124 (2024))
cGMP-konforme Reinigungsprozesse und deren Validierung / in der Sterilproduktion gemäß Annex 1 und Annex 15 · Schwarz R · GXP-TrainCon e.U., Wien
Reinigungsvalidierung Annex 1 Annex 15 Kreuzkontamination Kontaminationskontrollstrategie Dieser Beitrag soll Reinigungsprozesse im Umfeld der pharmazeutischen Produktion und somit in GMP-regulierten Bereichen betrachten. Spätestens mit Erscheinen des revidierten Annex 1 [ 1 ] zum EU-GMP-Leitfaden im Aug. 2022 kommt dem nahezu allumfassenden Thema „Kontaminationskontrolle“ eine gewichtige Rolle im Rahmen der Herstellung von sterilen Produkten zu. Explizit wird hierbei eine Umsetzung von Strategien, u. a. der Kontaminationskontrollstrategie („contamination control strategy“), auf die Herstellung nicht steriler Darreichungsformen von Pharmazeutika erwähnt und somit auch empfohlen. Generell sind hier Reinigungsprozesse an verschiedenen Stellen gefordert. In diesem Kontext ist auch die Reinigung produktberührender Equipmentoberflächen, die im Rahmen der ...
Sie sehen Artikel 11101 bis 11110 von insgesamt 12113
- Erste Seite
- 1109
- 1110
- 1111
- 1112
- 1113
- Letzte Seite