Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12022 Beiträge für Sie gefunden
-
High Voltage Leak Detection: Einfluss auf die Qualität von Biopharmazeutika
Rubrik: Originale
(Treffer aus pharmind, Nr. 01, Seite 114 (2019))
Scherer N | Ruthig P | Castelanelli M | Krüger T | Marcsekova K | Krumbein F | Cataldo P | Posset T
High Voltage Leak Detection: Einfluss auf die Qualität von Biopharmazeutika / Integritätsprüfung des Primärpackmittels steriler Arzneiformen mittels Hochspannung · Scherer N, Ruthig P, Castelanelli M, Krüger T, Marcsekova K, Krumbein F, Cataldo P, Posset T · Roche Diagnostics GmbH, Mannheim und und
High Voltage Leak Detection Container Closure Integrity Proteinoxidation/-denaturierung Ozon Temperaturanstieg Die Integrität von Primärverpackungen (CCI) parenteraler Lösungen ist von wesentlicher Bedeutung für die Qualität des sterilen Produkts. Durch eine integre Verpackung wird einerseits vor Verlust von Produkt und anderseits vor Kontaminationen von außen, durch eintretende Mikroorganismen, Gase und Schmutz geschützt. Um die Sicherheit des Patienten zu gewährleisten, wird daher zusätzlich zur Stabilitätsprüfung des Produkts eine 100-%-Dichtigkeits-Überprüfung gefordert [ 1 ]. Für diese von den Aufsichtsbehörden in den Vereinigten Staaten [ 2 ] und der Europäischen Union [ 3 ] vorgegebene vollständige Überprüfung ist eine zerstörungsfreie Messmethode vonnöten. Hierfür werden aktuell ...
-

Why has Mutual Recognition never become common practice for Homeopathic Medicinal Products?
Rubrik: Originale
(Treffer aus pharmind, Nr. 01, Seite 104 (2019))
Why has Mutual Recognition never become common practice for Homeopathic Medicinal Products? / The two pioneer cases of Mutual Recognition/Decentralised Procedures with homeopathic medicinal products in the simplified registration – Part 1 · Klein G, Sprenger A · 1Deutsche Homöopathie-Union DHU-Arzneimittel GmbH & Co. KG, Karlsruhe und Weleda AG, Schwäbisch Gmünd
Mutual Recognition Procedure Decentralised Procedure Homeopathic Medicinal Product Simplified Registration Deregulation This publication presents the experiences of the first 2 European multi-state registration procedures according to Chapter 4 of Directive 2001/83/EC executed with homeopathic medicinal products (HOMPs). Obtaining registrations for this category of medicinal products presents particular challenges related to their characteristics and market situation ( fig. 1 ). This is considered in the European law by definition of special registration procedures for HOMPs ( fig. 2 ). According to the legal definition, homeopathic medicinal products (HOMPs) are prepared according to homeopathic manufacturing procedures laid down in the European Pharmacopoeia or in an official ...
-

Facetten pharmazeutischer Mikrobiologie
Rubrik: Analytik / Betriebshygiene
(Treffer aus pharmind, Nr. 01, Seite 99 (2019))
Facetten pharmazeutischer Mikrobiologie / Zwischen Kontaminationsdogma, Nützlichkeit und Schönheit · Beckmann G · Institut Romeis Bad Kissingen, Oberthulba
Die pharmazeutische Mikrobiologie befindet sich in einem grundsätzlichen Dilemma. Einerseits häufig wenig beachtet oder nur unter dem Kontaminationsaspekt betrachtet, offenbart sie bei genauem Hinsehen doch auch viele nützliche, bisweilen sogar ästhetische Gesichtspunkte. Zeit, sich von einseitigen Betrachtungsweisen an vielen Stellen zu lösen.
-
Serie: Kalte WFI-Herstellung
Rubrik: Maschinen- und Anlagenbau
(Treffer aus TechnoPharm, Nr. 01, Seite 36 (2019))
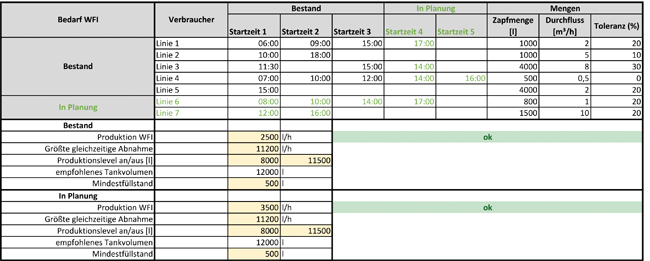
Serie: Kalte WFI-Herstellung / Teil 2*Teil 1 dieser Serie ist erschienen in TechnoPharm 8, Nr. 1, 12–17 (2018).: Lager- und Verteilsystem: Von Best-Practice-Ansätzen in etablierten HPW-Systemen bis zur modernen Biofilmkontrollstrategie · Rücker T · Letzner Pharmawasseraufbereitung GmbH, Hückeswagen
Kaltes WFI Biofilmkontrollstrategie Hygienic Design Zapfstellenmanagement Annex 15 Die kalte WFI-Erzeugung stellt sich aufgrund ihrer jungen Geschichte in Europa und der fehlenden Erfahrung mit entsprechenden Erzeugeranlagen als anspruchsvoll dar. Die Erfahrung mit Highly-Purified-Water(HPW)-Systemen hat über viele Jahre hinweg jedoch gezeigt, dass der Prozess beherrscht wird und somit die Technologie hierzu vorhanden ist. Eine Grundmotivation, die Technologie voranzutreiben, ist es, Energie zu sparen. Dass dieses Konzept energetisch noch attraktiver wird, indem das Water for Injection (WFI) zusätzlich auch entsprechend kalt gelagert und verteilt wird, versteht sich von selbst. Somit wird neben der sicheren Herstellung per Destillation die nächste Sicherheitsmaßnahme der bisherigen ...
-
Lagerung und Transport von Arzneimitteln
Rubrik: GMP-Aspekte in der Praxis
(Treffer aus pharmind, Nr. 01, Seite 90 (2019))
Lagerung und Transport von Arzneimitteln / Teil 2: Risikobetrachtung und Fallstudie für eine Lagerung < 15–25 °C*Teil 1 dieser Serie s. Pharm. Ind. 2018;80(10):1410–1416. · Frick C, Borchert D · 1kohlpharma GmbH, Merzig und Maas & Peither AG GMP-Verlag, Schopfheim
Im ersten Teil dieses Beitrags wurde dargelegt, dass der Temperaturbereich von 15–25 °C für die Lagerung und den Transport sog. „Standardarzneimittel“ in den GMP/GDP-Regularien nicht konkret gefordert wird. Darüber hinaus gibt es aus wissenschaftlicher Sicht keine Begründung für die Temperaturuntergrenze von 15 °C. In diesem Teil soll nun untersucht werden, welche Risiken mit einer Lagerung < 15 °C verbunden sind. Außerdem wird eine Fallstudie zu dieser Thematik vorgestellt.
-

The Asia Pacific Region
Rubrik: Ausland
(Treffer aus pharmind, Nr. 01, Seite 84 (2019))
Wittner
The Asia Pacific Region / Part 2: CMC Requirements during New Drug Application and Post-Approval Life-Cycle-Management in ASEAN Member States*Part 1 of this series see Pharm. Ind. 2018;80(3):391–397. · Wittner** These authors contributed equally to this work. ** These authors contributed equally to this work.
Part 2 is the second article in a series discussing requirements on Chemistry, Manufacturing and Control (CMC) of New Drug Applications (NDAs) and Post-Approval Life-Cycle-Management in the Asia Pacific Region and focuses on requirements within the Association of Southeast Asian Nations (ASEAN). Established in 1967 by five original members, ASEAN comprises ten member states (i.e. Malaysia, Indonesia, Thailand, the Philippines, Singapore, Brunei, Vietnam, Laos, Cambodia, and Myanmar) seeking to promote cooperation to accelerate economic growth and improve competitiveness through elimination of trade barriers and establishment of the ASEAN Free Trade Area (AFTA). AFTA has a population of 622 million people and a ...
-
SCHOTT – Plattformlösungen für Biotech-Medikamente
Rubrik: Unternehmensprofile
(Treffer aus pharmind, Nr. 01, Seite 80 (2019))
SCHOTT – Plattformlösungen für Biotech-Medikamente / pharmind • Unternehmensprofile
Selbst schwerwiegende Krankheiten lassen sich heute mit innovativen Medikamenten oder neuen Ansätzen der Zell- oder Gentherapien gut behandeln. Allerdings sind diese sogenannten Biologics aufgrund ihrer komplexen Molekularstruktur besonders empfindlich und tendieren dazu, mit dem Packmittel zu interagieren. Um sie stabil zu lagern und sicher zu verabreichen, sind deshalb besonders hochwertige Verpackungen notwendig. Darüber hinaus soll sich das Packmittel auf der Fülllinie gut prozessieren lassen und idealerweise eine genestete Ready-to-use-Abfüllung unterstützen. Wie lässt sich dies am besten erreichen? Basis für die Entwicklung pharmazeutischer Primärverpackungen ist eine vertrauensvolle und enge Zusammenarbeit von Pharmaunternehmen mit Verpackungsexperten, Elastomerproduzenten, Maschinenbauern und Device-Herstellern. Auf diese Weise ... -
Compliance im Reinraum durch Überwachung
Rubrik: Reinraum
(Treffer aus TechnoPharm, Nr. 01, Seite 30 (2019))
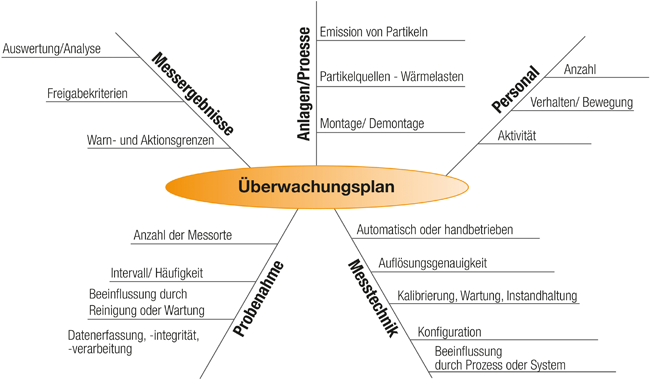
Compliance im Reinraum durch Überwachung / Praktische Umsetzung der Forderungen aus DIN EN ISO 14644-2:2016 – Teil 1 · Erens S · Testo Industrial Services GmbH, Kirchzarten
DIN EN ISO 14644 Reinräume Klassifizierung der Luftreinheit Überwachung Qualifizierung von Reinräumen Monitoring Der im Mai im DIN erschienene zweite Teil der ISO-14644-Normenreihe unterscheidet sich fundamental von der Vorgängerversion aus dem Jahr 2001 (DIN EN ISO 14644-2:2001-02 [3]). Während die Vorgängerversion als klassisches Vorgabedokument die durchzuführenden Prüfungen und Zuordnung der Intervalle beschreibt, verfolgt die aktuelle Version der ISO 14644-2 einen ganzheitlichen Ansatz, der auf die Leistungsfähigkeit des Reinraums oder des reinen Bereichs abzielt. Die Eignung eines Reinraums oder reinen Bereichs bzw. seine Performance soll mittels einer Überwachungsstrategie neben der erstmaligen oder regelmäßigen Durchführung von Klassifizierungsmessungen nachgewiesen werden. Ziel der Norm ist es, eine möglichst umfassende Zustandsbeschreibung für ...
-

Aktivitäten des PRAC
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 78 (2019))
Aktivitäten des PRAC / Aktuelle Empfehlungen des Ausschusses für Risikobewertung im Bereich der Pharmakovigilanz der Europäischen Arzneimittel-Agentur (EMA) · Thurisch B, Sickmüller B · Bundesverband der Pharmazeutischen Industrie (BPI) e. V., Berlin
Nähere Einzelheiten zu den aktuellen Verfahren und den Empfehlungen des PRAC sowie ergänzende Definitionen stehen auf der EMA-Webseite www.ema.europa.eu und im Hinblick auf die deutsche Übersetzung auf den Webseiten der deutschen Zulassungsbehörden Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM, www.bfarm.de /DE/Arzneimittel/Pharmakovigilanz/_node.html ) und Paul-Ehrlich-Institut (PEI, www.pei.de/DE/home/de-node.html ) zur Verfügung. In der Sitzung vom 26.–29. Nov. 2018 wurden keine neuen Referral-Verfahren initiiert oder abgeschlossen. Der aktuelle Stand der laufenden Referral-Verfahren im Bereich der Pharmakovigilanz ist Tab. 1 zu entnehmen. Produkt Verfahrenstyp Status Update weiterführende Informationen Methotrexate Art. 31 Under evaluation PRAC continued its assessment. Pharm. Ind. 2018 Mai;80(5):646. Anmerkungen Die jeweils ...
-

Aktivitäten des COMP
Rubrik: europharm
(Treffer aus pharmind, Nr. 01, Seite 72 (2019))
Aktivitäten des COMP / Throm • COMP · Throm S · Geschäftsführer Forschung, Entwicklung, Innovation vfa – Die forschenden Pharma-Unternehmen, Berlin
Vom 6.–8. Nov. und 4.–6. Dez. 2018 fanden bei der Europäischen Arzneimittel-Agentur (EMA) in London die 205. und 206. Sitzung des Ausschusses für Arzneimittel gegen seltene Krankheiten (Committee for Orphan Medicinal Products, COMP) statt. Dabei verabschiedete der Ausschuss: 21 bzw. 11 Empfehlungen für die Zuerkennung des Orphan-Status für die folgenden in Entwicklung befindlichen Medikamente: Acetylcystein zur Behandlung von Pseudomyxoma peritonei; MUCPharm Adeno-assoziierter viraler Vektor, der die humane 21-Hydroxylase exprimiert, zur Behandlung der ererbten adrenalen Hyperplasie; Pharma Gateway Afatinib zur Behandlung von Fanconi-Anämien; Consorcio Centro de Investigación Biomédica en Red, M. P. Bromelain zur Behandlung von Pseudomyxoma peritonei; MUCPharm humaner monoklonaler Antikörper gegen Promyostatin zur Behandlung der ...
Sie sehen Artikel 3421 bis 3430 von insgesamt 12022
- Erste Seite
- 341
- 342
- 343
- 344
- 345
- Letzte Seite