Ihr Suchergebnis
Sie recherchieren derzeit unangemeldet.Melden Sie sich an (Login) um den vollen Funktionsumfang der Datenbank nutzen zu können.
In der Rubrik Zeitschriften haben wir 12086 Beiträge für Sie gefunden
-

Alles im Fluss?
(Treffer aus cleanroom & processes, Nr. 02, Seite 107 (2024))
Alles im Fluss? / Ultraschall-assistierte Dekontamination für Isolatoren · Ludwig T
Beim Einsatz vernebelten Wasserstoffperoxids ist die gleichmäßige Verteilung des Desinfektionsmittels kritisch. Forschende der Universität Tokyo haben nun simuliert, wie Ultraschall dabei helfen kann. Isolatoren und Barrieresysteme müssen regelmäßig dekontaminiert werden. Im Pharma-Bereich kommt dafür hauptsächlich verdampftes (vapor phase hydrogen peroxide, VPHP) oder vernebeltes (aerosol hydrogen peroxide, AHP) Wasserstoffperoxid (H 2 O 2 ) zum Einsatz. Die Verwendung von AHP hat zwar einige Vorteile gegenüber VPHP, doch die Reichweite des reinigenden Nebels ist begrenzt. Studien zeigen, dass der Dekontaminationseffekt mit zunehmender Entfernung von der Injektionsstelle des AHP abnimmt. Die homogene Verteilung des Wasserstoffperoxidnebels ist also kritisch. Eine vielversprechende Methode hierfür ...
-
Eingebettete Prozessanalysetechnik in der kontinuierlichen Tablettenproduktion
Rubrik: Analytik
(Treffer aus Tech4Pharma, Nr. 02, Seite 106 (2024))
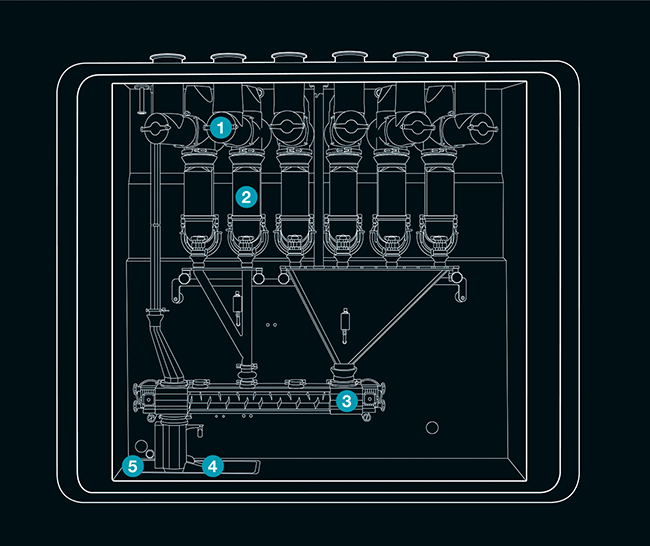
Eingebettete Prozessanalysetechnik in der kontinuierlichen Tablettenproduktion / Inline-Prozessüberwachung durch vollständig integrierte spektroskopische Instrumente · Geiger J, Novikova A · Fette Compacting, Schwarzenbek
Eingebettete Prozessanalysetechnik (ePAT) Kontinuierliche Produktion Tablettenproduktion Direktverpressung Nahinfrarotspektroskopie (NIRS) Marktforscher prognostizieren bis 2027 bei der kontinuierlichen Produktion (Continuous Manufacturing, CM) für die Pharmaproduktion ein überdurchschnittliches Wachstum von jährlich rund 10 % [ 1 ]. Auch die Lebens- und Arzneimittelbehörde der USA (Food and Drug Administration, FDA) sieht in der kontinuierlichen Herstellung ein entscheidendes Werkzeug zur Modernisierung der pharmazeutischen Industrie [ 2 ]. Ein wesentlicher Grund dafür sind demnach Verbesserungen bei der Produktqualität und der Patientensicherheit in Folge einer häufig erhöhten Prozesskontrolle. Darüber hinaus weisen kontinuierliche Verfahren gegenüber Batch-to-Batch-Produktionen grundsätzliche Vorteile auf: Neben der erhöhten Prozesssicherheit und Effizienz durch integrierte Prozesse ...
-
Präsenzschulungen sind besonders wertvoll – v. a. für Reinraumpersonal!
Rubrik: Reinraumkontext
(Treffer aus cleanroom & processes, Nr. 02, Seite 102 (2024))
Präsenzschulungen sind besonders wertvoll – v. a. für Reinraumpersonal! / Beckmann • Präsenzschulungen · Beckmann G · Institut Romeis Bad Kissingen, Oberthulba
Erwachsenengerechtes Lernen Präsenzschulung Onlineschulung Erfolgskontrollen Erwachsenenpädagogik In der pharmazeutischen Industrie inkl. der dort betriebenen Reinräume besteht eine regulatorische Verpflichtung zu regelmäßigen Schulungen und folgenden Erfolgskontrollen [ 1 ]. Dies wird den zunehmend arbeitsteiligen und komplexeren Aufgaben der zu Schulenden in verschiedenen Produktionszweigen gerecht – man denke nur an die Sterilfertigung und verschiedene „Entwicklungsstufen“ der Reinraumtechnik. Dass der arbeitende Mensch lebenslanger Fort- und Weiterbildung bedarf, ist in Zeiten eines beschleunigten Struktur- und Methodenwandels sowie epochalen Änderungen in der Arbeitswelt (Stichwort: Digitalisierung) und dem fortwährenden Zwang zur Ausbildung von Mitarbeitern On-the-Job aufgrund der Marktlage (Fachkräftemangel, Kostendruck usw.) unausweichlich und aus Qualitäts- und ...
-
Einbindung von Gefriertrocknern in den aseptischen Fertigungsprozess
Rubrik: Maschinen- und Anlagenbau
(Treffer aus Tech4Pharma, Nr. 02, Seite 100 (2024))
Einbindung von Gefriertrocknern in den aseptischen Fertigungsprozess / Bieler und Fischer • Gefriertrockner · Bieler S, Fischer F · PPT Pharma Process Technology GmbH, Frankfurt am Main
Gefriertrocknung Prozessführung Reinraum Aseptische Abfülllinie Barrieresysteme Die Gefriertrocknung wird in der pharmazeutischen Industrie seit vielen Jahren eingesetzt, um die Haltbarkeit sensitiver Produkte zu verlängern, indem den thermolabilen Wirkstoffen das Lösungsmittel (meist Wasser) entzogen wird. Typische im Pharmabereich gefriergetrocknete Produkte sind solche, die sich bei erhöhten Temperaturen zersetzen oder denaturieren, wie etwa Impfstoffe, Antibiotika, Seren oder proteinhaltige und biotechnologische Produkte. Bei der Gefriertrocknung, auch Lyophilisation genannt, wird die Produktlösung bei Atmosphärendruck eingefroren und anschließend ein Vakuum angelegt. Dabei geht das Lösungsmittel direkt von dem festen in den gasförmigen Zustand über. Diesen Vorgang bezeichnet man als Sublimation. Die Lyophilisation ist ein Teil ...
-
Schutz von kritischen Komponenten vor Oberflächenkontaminationen
Rubrik: Ausstattung
(Treffer aus cleanroom & processes, Nr. 02, Seite 96 (2024))
Kopp A | Moschner C | Müller A
Schutz von kritischen Komponenten vor Oberflächenkontaminationen / Teil 2*Teil 1 dieses Beitrags s. cleanroom & processes 2024;3(1): 4–9. · Kopp A, Moschner C, Müller A · Dastex Reinraumzubehör GmbH & Co. KG, Muggensturm und OHB System AG, Bremen
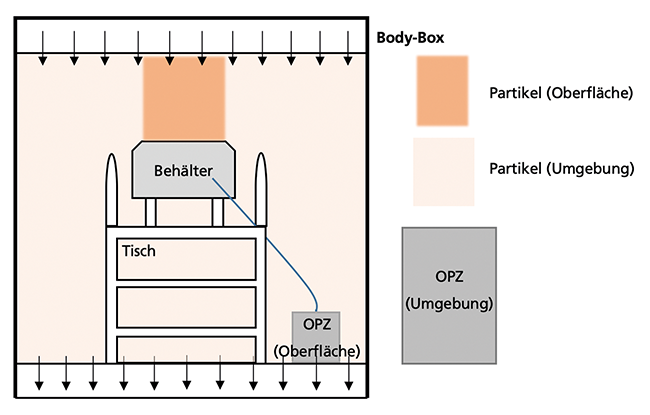
Der erste Teil der Versuche wurde in der Dastex Body-Box durchgeführt. Dabei handelt es sich um einen definierten, laminar durchströmten Reinraum mit Partikel-Monitoring, in welchem Vergleichsstudien durchgeführt werden können. Abbildung 7 zeigt schematisch den Aufbau. Als kritisches Objekt wurde ein Edelstahlbehälter eingesetzt, welcher gut ausgemessen und in den Ausgangszustand zurückversetzt werden kann. Der Behälter wurde mit einem Loch versehen, sodass eine isokinetische Sonde darin platziert werden konnte. Durch die Isokinetik wird sichergestellt, dass die luftgetragenen Partikel, welche sich oberhalb der kritischen Oberfläche befinden, dem Partikelzähler zur Detektion zugeleitet werden [ 2 ]. Durch diesen optischen Partikelzähler (OPZ) erfolgte die Detektion der ...
-
High-pressure cleaning in pharmaceutical production – a hitherto unjustly neglected technology!
Rubrik: Maschinen- und Anlagenbau
(Treffer aus Tech4Pharma, Nr. 02, Seite 92 (2024))
High-pressure cleaning in pharmaceutical production – a hitherto unjustly neglected technology! / Advantages and huge potential of sustainability and savings · Scheibel R · Tecniplast Deutschland GmbH, Hohenpeißenberg
high-pressure cleaning cGMP cleaning cleaning automation IBC cleaning system CIP/COP Automation of the cleaning of parts and tools coming from the production of pharmaceutical manufacturing became quite a standard within Good Manufacturing Practice (GMP) productions. Through fully validated cleaning processes and applications, safety could be achieved regarding cleaning success. Current Good Manufacturing Practice (cGMP) parts- and container-washers are available with different sizes of enclosed washing chambers that ensure cleaning success in pharmaceutical production under fully qualified status ( fig. 1 ). Nevertheless, there are applications and parts that cannot be applied to such a washing system because of their size or ...
-

Realisierung von Gefriertrocknungsanlagen
Rubrik: Planung
(Treffer aus cleanroom & processes, Nr. 02, Seite 90 (2024))
Realisierung von Gefriertrocknungsanlagen / Aktuelle regulatorische Anforderungen an Reinraumtechnologien zur aseptischen Prozessführung – Teil 1 · Bieler S, Mezricky P · PPT Pharma Process Technology GmbH, Frankfurt am Main
Gefriertrocknung Richtlinien Compliance Reinraumtechnologien Aseptische Prozessführung Reinraumtechnologien sind entscheidend, um eine kontrollierte Umgebung für die Produktion und Abfüllung von Arzneimitteln zu schaffen und Verunreinigungen zu minimieren, da diese die Wirksamkeit und Sicherheit beeinträchtigen können. Mikrobielle Kontaminationen führen zu Gesundheitsrisiken für Patienten, weshalb strenge regulatorische Anforderungen (Good Manufacturing Practice, GMP) gelten. Reinraumtechnologien gewährleisten eine stabile Produktionsumgebung, die sich positiv auf die Stabilität von empfindlichen Arzneimitteln auswirkt. Obwohl die Einführung Kosten verursacht, werden diese durch die Vermeidung von Produktverlusten und Produktionsausfällen oft ausgeglichen. Die Nachfrage nach sicheren Reinraumumgebungen (insbesondere für die Produktion von Impfstoffen und anspruchsvollen Arzneimitteln) steigt und hat Auswirkungen auf ...
-
Sicherheitswerkbänke zur aseptischen Aufbereitung patientenindividuell dosierter Zubereitungen
Rubrik: Technik
(Treffer aus cleanroom & processes, Nr. 02, Seite 84 (2024))
Sicherheitswerkbänke zur aseptischen Aufbereitung patientenindividuell dosierter Zubereitungen / Case Study der Anstaltsapotheke des Pyhrn-Eisenwurzen Klinikums (PEK) Steyr · Hein R · Oberösterreichische Gesundheitsholding GmbH, Steyr
EU-GMP-Leitfaden Annex 1 Sicherheitswerkbank Patientenindividuelle aseptische Zubereitung Isolator RABS In Österreich wird der Betrieb von Apotheken durch die Apothekenbetriebsordnung 2005 [ 3 ] reglementiert. Apotheken, die eine Bewilligung nach § 63 Arzneimittelgesetz [ 4 ] führen, unterliegen den Vorschriften der Arzneimittelbetriebsordnung [ 5 ] und müssen ebenso wie die pharmazeutische Industrie die Vorgaben der Richtlinien bzgl. Good Manufacturing Practice (GMP) erfüllen [ 6 ]. Die seit 25.08.2023 gültige Revision des Annex 1 des EU-GMP-Leitfadens stellt neue, z. T. höhere Anforderungen. Diese betreffen nicht nur die Prozesse an sich, sondern auch die bauliche und technische Ausstattung. Krankenhausapotheken unterscheiden sich in ihrer Funktion und den daraus ...
-
Serie: Beschaffen und Betreiben vorqualifizierter Teilanlagen
Rubrik: Automation
(Treffer aus Tech4Pharma, Nr. 02, Seite 84 (2024))
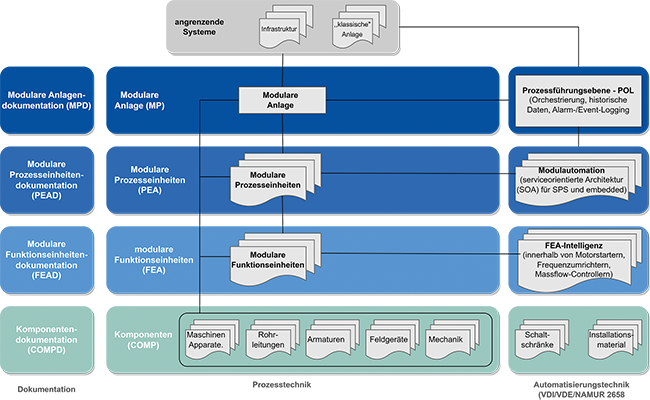
Serie: Beschaffen und Betreiben vorqualifizierter Teilanlagen / Teil 2*Teil 1 dieser Serie s. Tech4Pharma 2024;14(1):18–25.: Integrierte Equipment-Qualifizierungs- und Validierungsstrategie computergestützter Systeme für modulare Anlagen · Makait T · Thomas Makait QPRI – Transparenz für Projekteffizienz, Hofheim am Taunus
Modulare Anlagen PEA,MTP,POL Qualifizierung Equipment Validierung computergestützter Systeme Anlagenqualifizierung Im 1. Beitrag wurden die wesentlichen Schritte zur Flexibilisierung und Effizienzsteigerung in der pharmazeutischen Prozessindustrie durch das Beschaffen und Betreiben von vorqualifizierten Teilanlagen dargestellt. Es wurden erforderliche Schritte beschrieben, um dieses Potenzial zu heben und geeignete Vorgehensweisen zur abteilungs- und organisationsübergreifenden Zusammenarbeit zu etablieren. Im 3. Beitrag werden die erforderlichen Schritte zum Beschaffen und Integrieren von durch PEA-Hersteller vorqualifizierten Process Equipment Assemblies (PEAs) beschrieben, um dabei QA-Oversight des Betreibers sicherzustellen. Im 4. Beitrag werden die wesentlichen Aspekte zum Qualifizieren und Betreiben modularer Anlagen (MP) bestehend aus vorqualifizierten PEA beschrieben. Die beschriebene Vorgehensweise basiert im ...
-
Druckluft im Reinraum
Rubrik: Technik
(Treffer aus cleanroom & processes, Nr. 02, Seite 80 (2024))
Druckluft im Reinraum / Werner • Druckluft · Werner D · Hanns G. Werner GmbH + Co. KG, Tornesch
Druckluft Reinraum Annex 1 Partikeleintrag Luftkeimzahl Druckluftanwendungen im Reinraum stellen für die Qualifizierung eine besondere Herausforderung dar [ 1 ]. Druckluft gilt als ein sauberer Energieträger und hat für verschiedene Aufgaben Vorteile gegenüber alternativen Lösungen. Die möglichen Anwendungen sind vielfältig: pneumatische Schalt- und Transportvorgänge (wie Pusher), Druckbeaufschlagung von Sterilfiltern, Ausblasen von leeren Ampullen zur Trocknung nach dem Waschen, Kunststoffausformung in Formen (Blow-Fill-Seal), Abdichtung von Schleusenöffnungen mit Druckluftmanschetten, Abblasen von Produktoberflächen zur letzten Abreinigung von Partikeln, um nur einige Beispiele zu nennen. Dabei unterscheidet man zunächst 2 Situationen: Wird die Druckluft lediglich in einem geschlossenen System in den Reinraum ein- und wieder ...
Sie sehen Artikel 1001 bis 1010 von insgesamt 12086
- Erste Seite
- 99
- 100
- 101
- 102
- 103
- Letzte Seite